アミロイドβとは? ― アルツハイマー型認知症の原因物質を分かりやすく解説
認知症予防の話題でたびたび登場する「アミロイドβ」
認知症は、いまや一人ひとりの健康の問題にとどまらず、医療・介護・経済、そして家族のかたちにまで影響が及ぶ大きな社会課題となっています。2024年には「共生社会の実現を推進するための認知症基本法」が施行され1、国や自治体、企業が一体となって「共生」と「予防」の両輪で向き合う姿勢が明確に打ち出されました。
研究・医療の世界では、アルツハイマー型認知症の原因物質とされる「アミロイドβ」を標的にした抗体医薬※が登場し、日本でも保険適用が始まりました2。一方で、その効果や副作用をめぐる議論は現在も続いており3、薬だけに頼らない「予防」と「早期発見」への関心が、高まっています。
 用語解説
用語解説
- 抗体医薬
- 体内の特定の物質(抗原)にだけ結合する「抗体」を人工的につくって投与する薬。
「アミロイドβ」という言葉は耳にしたことがあっても、実際にどんなものか説明できる人は意外と少ないのではないでしょうか。本記事では、アミロイドβがどういうもので、なぜ脳に溜まるのか、加齢や生活習慣とどう関係するのか、そして近年注目される「タウ」との関係までを、分かりやすく解説します。
この記事でわかること
- アミロイドβとは?脳内のタンパク質から切り出される短いペプチドで、凝集すると「老人斑」をつくる
- なぜ問題なのか?神経細胞を傷つけ、症状が出る20〜30年前から蓄積が始まる
- アミロイドβだけではない ― もう一つの原因タンパク質「タウ」
- 脳の老化を防ぐ・遅らせるために日常でできること
アミロイドβとは?
アミロイドβ(Amyloid β、Aβ)とは、「アミロイド前駆体タンパク質(APP)」から切り出される短いペプチドの総称です。これが異常に凝集すると不溶性の塊となり、アルツハイマー型認知症の患者さんの脳に多く見られる「老人斑(ろうじんはん)」の主成分となります。
アミロイドβができるまで
アミロイドβは、「アミロイド前駆体タンパク質(APP:Amyloid Precursor Protein)」という、もともと神経細胞の表面に存在する大きなタンパク質から、複数の酵素(セクレターゼ)によって切り出されて生まれます。
健康な状態では、APPは主にα/γセクレターゼ経路※によって無害な短い断片に分解され、問題を起こしません。しかし加齢などによってβ/γセクレターゼ経路※の働きが優位になると、「アミロイドβ42(Aβ42:アミノ酸42残基からなる、特に凝集しやすい型)」が多く作られるようになります。この断片同士が凝集し、最終的に老人斑と呼ばれる沈着物を形成すると考えられています4。
 用語解説
用語解説
- α/γセクレターゼ経路
- APPを「α-セクレターゼ」と「γ-セクレターゼ」という2つの酵素が順に切り分ける経路。途中でアミロイドβは生まれず、いわば「安全な切り分け方」とされる。
- β/γセクレターゼ経路
- APPを「β-セクレターゼ」と「γ-セクレターゼ」が順に切り分ける経路。途中でアミロイドβが切り出されるため、加齢や遺伝的要因などでこちらが優位になると蓄積につながると考えられている。
健康な脳では日常的に「掃除」されている
実はアミロイドβは、健康な脳でも日常的に作られています。通常は脳内の分解システムやミクログリア(脳の免疫細胞)、そしてオートファジーなどの仕組みによって速やかに除去されています5 6。
オートファジーについて詳しくは、「オートファジーとは?」をご覧ください。
バランスが崩れると蓄積が始まる
問題となるのは、「作られる量」と「分解される量」のバランスが崩れ、分解が追いつかなくなったときです。加齢に伴って分解系の働きが落ちると、長い年月をかけて脳内にアミロイドβが蓄積していきます7。
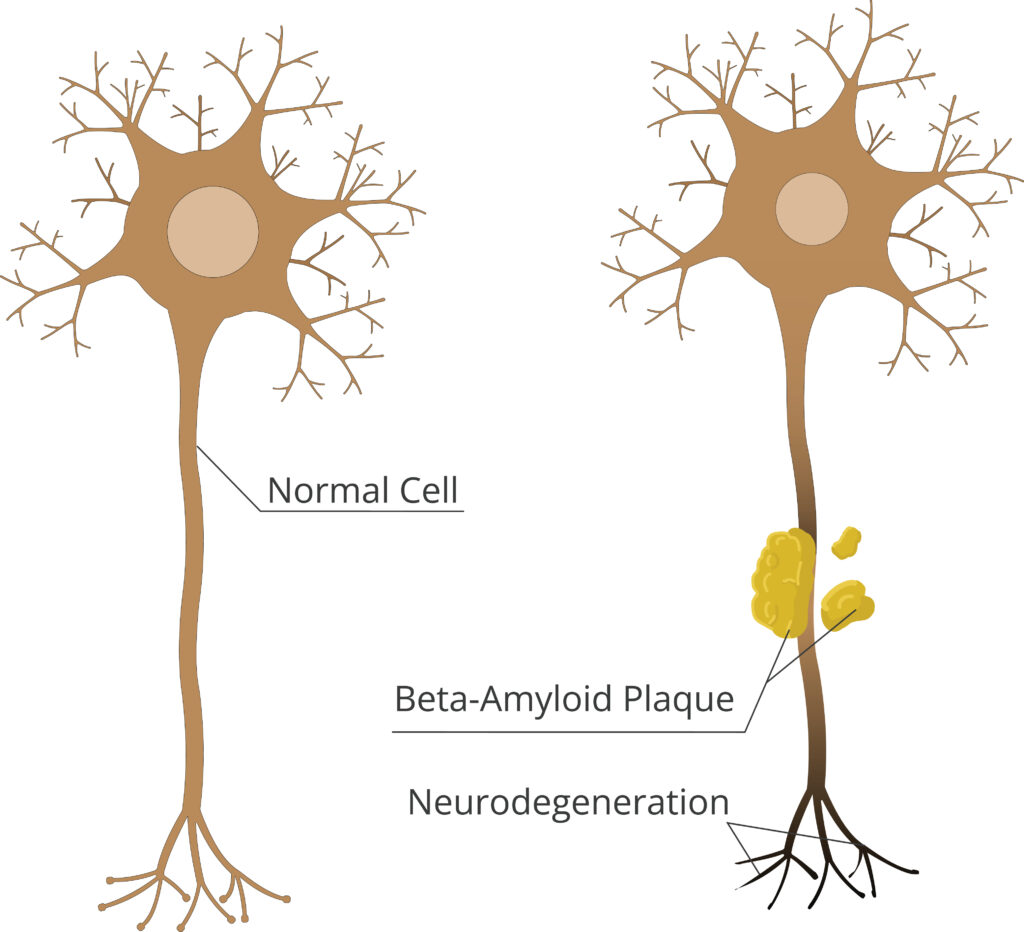
アミロイドβはなぜ問題なのか?
神経細胞を傷つける
凝集したアミロイドβは、神経細胞同士のつながり(シナプス)を障害し、情報伝達を乱すことが知られています8。さらに、凝集体の周囲では炎症が起こりやすく、最終的には神経細胞そのものを死に至らせる可能性があります9。その結果として、記憶や判断力といった認知機能が徐々に低下していくと考えられています。
症状が出る前から脳を蝕んでいる
特に注目すべきなのは、アミロイドβの蓄積が「認知症の症状」として表面化するずっと前から始まっている、という点です。
遺伝性アルツハイマー病の家系を長期追跡した国際共同研究「DIAN研究(Dominantly Inherited Alzheimer Network)」では、脳脊髄液※中のアミロイドβの変化が発症予測年齢の約25年前から、脳への沈着が約15年前から始まっていることが報告されました10。40代・50代で「最近物忘れが増えたな」と感じ始める頃には、脳内ではすでに何十年もかけてアミロイドβの蓄積が進行している可能性がある、ということです。
裏を返せば、症状が出る前の長い「予備期間」にどう過ごすかが重要ということでもあります。日々の生活習慣の積み重ねが、その後の脳の状態に少しずつ影響していくと考えられています。
 用語解説
用語解説
- 脳脊髄液
- 脳と脊髄のまわりを満たす透明の液体。脳内の状態を反映しやすく、神経疾患のバイオマーカー検査にも用いられる。
アミロイドβだけではない ― もう一つの原因タンパク質「タウ」
長年、アルツハイマー型認知症の研究では「アミロイドβこそが病気の原因」という考え方(アミロイド仮説)が中心でした11。しかし近年、アミロイドβを脳から除去する抗体医薬を開発しても、期待されたほど認知機能が改善しないケースが報告されるなど、アミロイドβだけでは病気の全体像を説明しきれないことが分かってきました12。こうした背景から、現在は「タウ」というもう一つのタンパク質や、神経炎症、血管性の要因、生活習慣など、複数の要因を合わせて考える多角的なアプローチが主流になりつつあります。
アミロイドβとタウの違い
アミロイドβとタウは、蓄積する場所も性質も異なります。
- アミロイドβ:神経細胞の外側に溜まり、「老人斑」をつくる
- タウ:神経細胞の内側に溜まり、糸くずが絡まったような「神経原線維変化※」をつくる
タウは本来、神経細胞内の微小管(細胞の骨組みを支える線維)を安定化させる役割を持つタンパク質ですが、過剰にリン酸化※が進むと微小管から離れ、絡まり合って細胞内に蓄積していきます13。
 用語解説
用語解説
- 神経原線維変化
- 過剰にリン酸化したタウが神経細胞の内部で絡まり合い蓄積した病変。老人斑(アミロイドβ)と並ぶ、アルツハイマー型認知症の代表的な病理所見のひとつ。
- リン酸化
- タンパク質にリン酸基が結合する反応。本来は生体内で正常に起こる反応だが、タウでは過剰なリン酸化(過リン酸化)が病的な凝集を引き起こす。
「p-tau217」という早期発見の指標
リン酸化されたタウのうち、とくに「p-tau217」と呼ばれる形は、アルツハイマー型認知症の進行度と強く相関することから、血液検査で測定できる早期バイオマーカーとして注目されています。米国では2025年、p-tau217とアミロイドβ42の比を指標とした初の臨床用血液検査が承認され、症状が出る前の段階からリスクを評価できる可能性が期待されています14。
こうしたバイオマーカー研究の進展は、症状が現れる前の段階からリスクを把握し、生活習慣の改善や早期介入につなげる道を開きつつあります。

脳の老化を防ぐ・遅らせるためにできること
では、その「生活習慣」として、私たちは日常で何を意識すればよいのでしょうか。ここからは、研究で裏付けが進んでいる「アミロイドβやタウの蓄積を抑え、脳の老廃物処理を助ける」ための3つのアプローチを紹介します。
質の良い睡眠
脳には「グリンパティックシステム※」と呼ばれる排出経路が備わっており、これは主に深い睡眠中に活発に働いてアミロイドβを洗い流していると考えられています15。睡眠不足が続くと脳内のアミロイドβ濃度が上昇しやすいという報告もあり、睡眠の量と質は認知症予防の土台となります。
 用語解説
用語解説
- グリンパティックシステム
- 脳内の老廃物を洗い流す、リンパ系のような仕組み。
適度な運動
有酸素運動は、脳の血流を増やすだけでなく、オートファジーの活性化や脳由来神経栄養因子(BDNF)の産生促進など、複数の経路で脳の健康維持に関わる可能性が報告されています16。激しい運動である必要はなく、ウォーキングや軽いジョギングなど、継続的に体を動かす習慣が、長期的な認知機能の維持につながる可能性があります17。
食事・栄養成分
食事面では、オートファジーの活性化が期待されるカロリー制限や間欠的ファスティング、抗酸化・抗炎症作用のある食品成分(緑黄色野菜、ベリー類、青魚など)が、認知機能維持の観点から研究対象として注目されつつあります18。
本わさび由来の希少成分「ヘキサラファン(6-MSITC)」は、Nrf2経路を活性化することで抗酸化・抗炎症作用を発揮することが知られています。ヒトを対象としたランダム化比較試験(RCT)では高齢者の記憶機能に対する有用性が報告されており19、詳細はこちらの記事で紹介しています。 また、タウの異常なリン酸化に対する食品成分の関与についても研究が進みつつあり、ヘキサラファンとタウ病理の関係はこちらの記事で紹介しています。
まとめ
- アミロイドβは、APP(アミロイド前駆体タンパク質)から切り出される短いペプチドで、異常に凝集すると「老人斑」を形成し、アルツハイマー型認知症の原因物質の一つとされる
- 症状が出る20〜30年前から蓄積が始まっており、早い段階からの予防的アプローチが重要
- 近年は、アミロイドβだけでなく「タウ」も含めた多角的な視点で研究が進んでいる
- 睡眠・運動・食事など日々の生活習慣が、蓄積のスピードや分解能力に影響する
「そもそもアミロイドβってなに?」と立ち返りたくなったときに、ぜひこの記事を読み直してみてください。
[ 引用・参考文献 ]
- 内閣府「共生社会の実現を推進するための認知症基本法」(令和5年法律第65号、2024年1月1日施行) ↩︎
- エーザイ株式会社・バイオジェン・ジャパン株式会社「抗アミロイドβ(Aβ)プロトフィブリル抗体レカネマブ(製品名:レケンビ®点滴静注)の日本における保険適用について」(2023年12月20日) ↩︎
- van Dyck CH, et al. “Lecanemab in Early Alzheimer’s Disease.” New England Journal of Medicine 388(1): 9–21 (2023) ↩︎
- Haass C, Selkoe DJ. “Soluble protein oligomers in neurodegeneration: lessons from the Alzheimer’s amyloid β-peptide.” Nature Reviews Molecular Cell Biology 8: 101–112 (2007) ↩︎
- Hickman SE, et al. “Microglial dysfunction and defective β-amyloid clearance pathways in aging Alzheimer’s disease mice.” Journal of Neuroscience 28(33): 8354–8360 (2008) ↩︎
- Nixon RA. “The role of autophagy in neurodegenerative disease.” Nature Medicine 19: 983–997 (2013) ↩︎
- Mawuenyega KG, et al. “Decreased clearance of CNS β-amyloid in Alzheimer’s disease.” Science 330(6012): 1774 (2010) ↩︎
- Selkoe DJ. “Alzheimer’s disease is a synaptic failure.” Science 298(5594): 789–791 (2002) ↩︎
- Heneka MT, et al. “Neuroinflammation in Alzheimer’s disease.” Lancet Neurology 14(4): 388–405 (2015) ↩︎
- Bateman RJ, et al. “Clinical and Biomarker Changes in Dominantly Inherited Alzheimer’s Disease.” New England Journal of Medicine 367: 795–804 (2012) ↩︎
- Hardy J, Selkoe DJ. “The amyloid hypothesis of Alzheimer’s disease: progress and problems on the road to therapeutics.” Science 297(5580): 353–356 (2002) ↩︎
- Nonino F, et al. “Amyloid-beta-targeting monoclonal antibodies for people with mild cognitive impairment or mild dementia due to Alzheimer’s disease.” Cochrane Database of Systematic Reviews 2026, Issue 4 ↩︎
- Wang Y, Mandelkow E. “Tau in physiology and pathology.” Nature Reviews Neuroscience 17: 5–21 (2016) ↩︎
- U.S. Food and Drug Administration. “FDA Clears First Blood Test Used in Diagnosing Alzheimer’s Disease.” Press Announcement (May 2025) ↩︎
- Xie L, et al. “Sleep Drives Metabolite Clearance from the Adult Brain.” Science 342(6156): 373–377 (2013) ↩︎
- Mesrabadi J, et al. “Exercise training alters resting brain-derived neurotrophic factor concentration in older adults: A systematic review with meta-analysis of randomized-controlled trials.” Ageing Research Reviews (2024) ↩︎
- Livingston G, et al. “Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission.” The Lancet 404(10452): 572–628 (2024) ↩︎
- Mattson MP, Arumugam TV. “Hallmarks of Brain Aging: Adaptive and Pathological Modification by Metabolic States.” Cell Metabolism 27(6): 1176–1199 (2018) ↩︎
- Nouchi R, et al. “Benefits of Wasabi Supplements with 6-MSITC (6-Methylsulfinyl Hexyl Isothiocyanate) on Memory Functioning in Healthy Adults Aged 60 Years and Older: Evidence from a Double-Blinded Randomized Controlled Trial.” Nutrients 15(21): 4608 (2023) ↩︎