NMNは腸内細菌を介してNAD+を高める – 最新研究が示した新しいメカニズム
私たちは、世界中の研究の指標となっている12の老化要因「AGING HALLMARKS」を研究の指針としています。12の老化要因の中でも、加齢にともなうエネルギー代謝の低下に深く関わる「NAD+の減少」は、健康長寿を考える上で避けては通れないテーマです。今回は、2026年1月に科学誌 Nature Metabolism に掲載された最新研究をご紹介します※1。この研究では、NMN(ニコチンアミドモノヌクレオチド)・NR(ニコチンアミドリボシド)・Nam(ナイアシンアミド)という3つのNAD+前駆体※2を、ヒトで初めて同一試験内で直接比較しました。この研究結果と、研究から見えてきた「腸内細菌を介したNAD+上昇メカニズム」という新発見について、わかりやすく解説します。
※2 その物質が生成される前段階の物質のこと
この記事でわかること
- NAD+とは何か、なぜ加齢とともに減少するのか
- NMN・NR・Namの3つのNAD+前駆体の違い
- 研究結果の紹介:NMNとNRが14日間でNAD+を有意に上昇させた
- 新発見:NMNとNRが腸内細菌によってニコチン酸(NA)に変換され、NAD+を持続的に高めるメカニズム
- 新しいモデル:腸を経由するNAD+上昇メカニズム
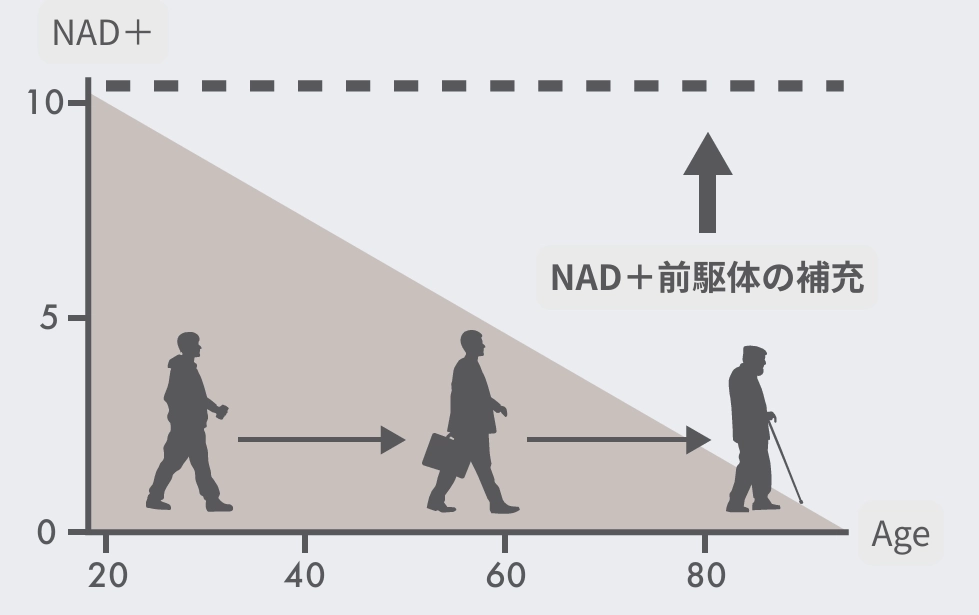
NAD+とは? ‐ 生命活動を支える「エネルギーのみなもと」
NAD+(ニコチンアミドアデニンジヌクレオチド)は、ビタミンB3をもとに体内で合成される補酵素※3です。エネルギー産生やDNA修復など、体内の数百もの代謝反応に関わっています。また、細胞の修復・老化防止に重要な「サーチュイン」というタンパク質を活性化するためにも欠かせません。この、NAD+は加齢とともに減少していくことがわかっています。※4。NAD+が減少すると、エネルギー代謝の低下、DNA修復力の衰え、炎症の増加など、さまざまな老化現象を引き起こすと考えられています。NAD+の減少を補う方法として注目されているのが、体内でNAD+に変換される「前駆体」を補給するアプローチです。
※3 酵素の働きを助ける物質のこと
3つのNAD+前駆体:NMN・NR・ナイアシンアミド
NAD+の主要な前駆体として、以下の3つが注目されています。
- NMN(ニコチンアミドモノヌクレオチド):NAD+の直接の前駆体。近年、サプリメントとして広く注目されています。
- NR(ニコチンアミドリボシド):NMNの一段階前の物質で、同様にNAD+の合成に寄与します。
- Nam(ナイアシンアミド):ビタミンB3の一種で、最も古くから知られるNAD+前駆体です。
【研究紹介】3つのNAD+前駆体をヒトで初めて直接比較した臨床試験
2026年1月、科学誌 Nature Metabolism に掲載された本研究は、NMN・NR・ナイアシンアミド(Nam)の3つのNAD+前駆体を、ヒトで初めて同一試験内で直接比較しました。本研究は大きく3つのパートで構成されています。
パート1:ヒト臨床試験
- 研究デザイン: ランダム化、オープンラベル、プラセボ対照試験(RCT)
- 対象: 健康な成人65名
- NMN、NR、Nam、プラセボの4群に分け、4群に分けて14日間毎日摂取:
- NMN群(1日1,000 mg、15名)
- NR群(1日1,000 mg、16名)
- Nam群(1日500 mg、17名)
- プラセボ群(17名)
- 測定: 全血中のNAD+と関連代謝物を、摂取前・摂取後4時間(急性効果)・14日後(慢性効果)に測定
パート2:腸内細菌の発酵実験(ex vivo)
- 健康な成人6名、クローン病患者10名、高齢者10名の便由来の腸内細菌を、NRやNamと48時間培養
- 腸内細菌がこれらの物質をどう代謝するか、また細菌の増殖や代謝活動への影響を観察
パート3:全血培養試験(in vitro)
- 健康な成人4名の全血に、NA・NAR・NAMN・Nam・NR・NMNの6種類のNAD+前駆体をそれぞれ加え、7時間にわたりNAD+の変化を追跡
実施機関: Nestlé Research(スイス・ローザンヌ)ほか
論文: Christen S. et al., Nat. Metab. 8(1):62-73, 2026(※1)
研究結果について
1. NMNとNRは14日間でNAD+を有意に上昇させた
14日間の継続摂取の結果、NMN群とNR群では血中のNAD+濃度がプラセボ群と比べて有意に上昇しました。一方、Nam群では有意な変化は認められませんでした。また、NMNとNRのNAD+上昇効果は同程度であることも確認されました。
2. Namは「急性効果」のみ、NMN・NRは「持続効果」
摂取直後(4時間以内)の「急性効果」を見ると、NamだけがNAD+代謝物に影響を与えました。しかしその効果は一過性であり、長期的なNAD+の上昇にはつながりませんでした。対照的に、NMNとNRは急性効果こそ小さいものの、14日間で持続的にNAD+を上昇させました。つまり、「飲んですぐ効く」ことと「長期的にNAD+を高める」ことは別の話であり、NMNとNRは日々の継続摂取によってこそ、その力を発揮するといえます。
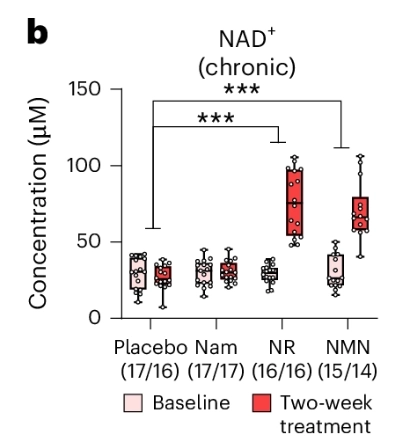
14日間服用前後の血中NAD+濃度を示した図 (出典: Christen, S. et al., Nat. Metab. 8(1), 62–73 (2026), Fig. 1b より引用)
図の見方:縦軸がNAD+濃度。横軸が偽薬(プラセボ)、NAD+前駆体それぞれの服用前と服用2週間後の濃度
3. 新発見:NMNとNRは腸内細菌によって「ニコチン酸(NA)」に変換される
ヒトの腸内細菌を用いた発酵実験(ex vivo=生体外で行う実験)では、NMNとNRが腸内細菌によってニコチン酸(NA)に変換されることが確認されました。さらに、NMNとNRは腸内細菌の増殖と代謝活動(短鎖脂肪酸の産生やガス産生)を促進させることも明らかになりました。
4. 全血実験でNAがNAD+上昇の鍵となる物質であることが判明
全血を用いた実験では、NAが他の前駆体と比べて顕著にNAD+を上昇させることが示されました。興味深いことに、NMN・NR・Namを直接血液に加えても、NAD+の上昇効果は限定的でした。つまり、NMNやNRは、腸内細菌によってNAに変換されてはじめて、効率的にNAD+を高めることができるのです。
新しいモデル:腸を経由するNAD+上昇メカニズム
これらの結果をもとに、研究チームは以下のモデルを提唱しています。
NMN・NR → 腸内細菌がNAに変換 → Preiss-Handler経路※5 → NAD+が持続的に上昇
Nam → 小腸で速やかに吸収 → サルベージ経路※6 → NAD+が一時的に上昇
従来、「NMNやNRは血液中に直接取り込まれ、そのままNAD+に変換される」と考えられてきました。しかし本研究では、NMNやNRがまず腸内細菌によってニコチン酸(NA)に変換され、その後に全身のNAD+を高めるという新たなメカニズムが明らかになりました。
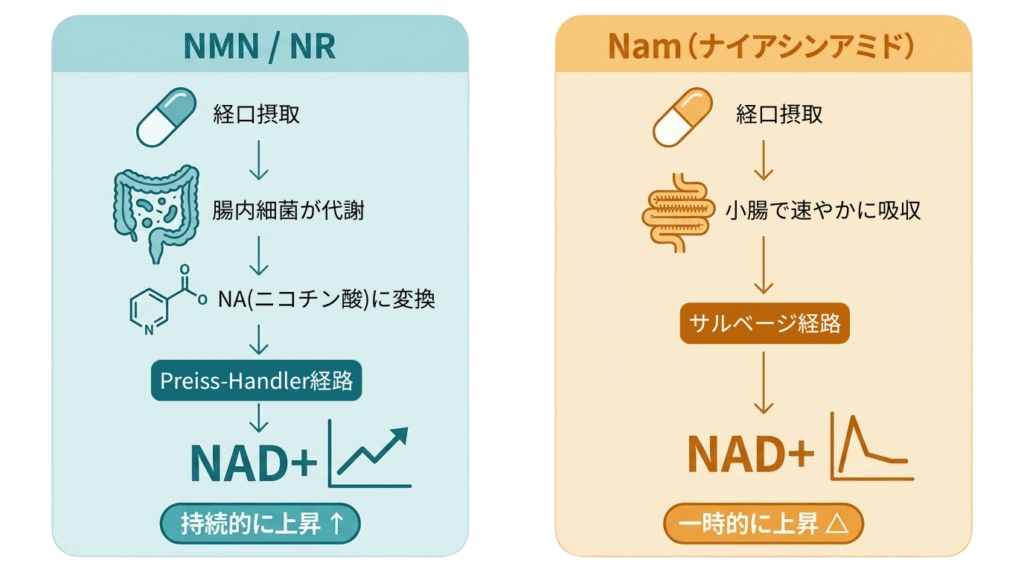
NMNとNRは、腸内細菌の力を借りてNAに変換され、「Preiss-Handler経路」(ニコチン酸からNAD+を合成する経路)と呼ばれるルートを通じて持続的にNAD+を高めます。一方、Namは小腸から速やかに吸収され、「サルベージ経路」(ナイアシンアミドを再利用してNAD+を合成する経路)を通じて一時的にNAD+に影響を与えますが、持続的な上昇にはつながりません。
※5 ビタミンB3の一種である「ニコチン酸(NA)」を出発点として、段階的にNAD+を組み立てていく体内の仕組みです。
※6 NAD+が体内で使われた後に生じる「ナイアシンアミド(Nam)」を回収し、再びNAD+へとつくり直すリサイクル経路です。
考察:この研究から見えてきたこと
NMNを「口から飲む」ことの重要性
本研究で特に注目すべきは、NMNやNRを直接血液に加えてもNAD+はほとんど上昇しなかったという全血培養実験の結果です。血液中ではNMNはCD38(NAD+分解酵素)によって速やかに分解され※7、NRもPNP※8によって処理されてしまいます※9。
では、NMNやNRはどうやってNAD+を高めていたのか。答えは「腸」にありました。口から摂取されたNMNやNRは、腸内細菌によってNA(ニコチン酸)に変換されます。このNAが血液に入り、全身のNAD+を持続的に押し上げていたのです。
この結果は、近年広まっているNMN点滴療法にも関わる話です。点滴では腸を通らないため、腸内細菌によるNA変換が起きません。本研究のモデルに基づけば、点滴では持続的なNAD+上昇は得られにくいと考えられます。
※8 NR(ニコチンアミドリボシド)からNam(ナイアシンアミド)に分解する働きを持つ酵素
「腸内環境」という新たな変数
NMNの効果が腸内細菌によるNA変換に左右されるなら、「腸内環境が違えば、NMNの効き方も変わるのでは?」という疑問も浮かびます。
- 腸内細菌叢が健全であれば → NA変換が効率よく進み、NAD+が上がりやすい
- 腸内環境が乱れていれば → 変換効率が低下する可能性がある
ただし、本研究では高齢者やクローン病患者の腸内細菌でもNA変換が確認されており、この経路がかなりタフであることも同時に示されています。とはいえ、NMNの恩恵を最大化するうえで「腸内環境を整える」ことが一つの重要な視点になる、というのは今後さらに掘り下げる価値のあるテーマです。
NMNの「プレバイオティクス的側面」という新発見
もう一つ見逃せないのが、NMNとNRが腸内細菌の増殖を促し、短鎖脂肪酸(SCFA)の産生を活性化したという発見です。SCFAは腸のバリア機能の免疫調節を支える物質として知られています※10※11。
つまり、NMNには二つの顔がある可能性が出てきました。
- NAを介した全身のNAD+上昇(代謝の改善)
- 腸内細菌の活性化とSCFA産生促進(腸内環境の改善)
NMNが「腸にも良い」という視点は、これまで見落とされてきました。今後のさらなるヒト臨床試験での検証が待たれます。
[ 引用・参考文献 ]
※1 Christen, S. et al. The differential impact of three different NAD+ boosters on circulatory NAD and microbial metabolism in humans. Nat. Metab. 8(1), 62–73 (2026).
※4 Migaud, M. E., Ziegler, M. & Baur, J. A. Regulation of and challenges in targeting NAD+ metabolism. Nat. Rev. Mol. Cell Biol. 25, 822–840 (2024).
※7 Sauve, A. A., Munshi, C., Lee, H. C. & Schramm, V. L. The reaction mechanism for CD38. A single intermediate is responsible for cyclization, hydrolysis, and base-exchange chemistries. Biochemistry 37, 13239–13249 (1998).
※9 Bzowska, A., Kulikowska, E. & Shugar, D. Purine nucleoside phosphorylases: properties, functions, and clinical aspects. Pharmacol. Ther. 88, 349–425 (2000).
※10 Bedani, R., Cucick, A. C. C., Albuquerque, M. A. C., LeBlanc, J. G. & Saad, S. M. I. B-group vitamins as potential prebiotic candidates: their effects on the human gut microbiome. J. Nutr. 154, 341–353 (2024).
※11 Krautkramer, K. A., Fan, J. & Bäckhed, F. Gut microbial metabolites as multi-kingdom intermediates. Nat. Rev. Microbiol. 19, 77–94 (2021).