本わさびの成分がアルツハイマー型認知症に効く?‐ヘキサラファンの最新研究を解説
日本は超高齢化社会に突入しています。厚生労働省の推計によると、2030年には認知症の人が約523万人、軽度認知障害(MCI)を含めると約1,116万人に達するとされています。2040年には、65歳以上の約3人に1人が認知症またはその予備軍になると算定されています1。認知症がもたらす社会的コストも深刻です。医療費・介護費・インフォーマルケアコストを合わせると年間14.5兆円(2014年時点)に上り、2060年には24.3兆円規模にまで膨らむと試算されています2。
認知症の約6〜7割を占めるアルツハイマー型認知症には、いまだ根本的な治療法が確立されていません。近年承認された抗体医薬(レカネマブなど)はアミロイドβの除去を目的としていますが、病気の進行を完全に止めるには至っていません。そのため研究領域では、発症前の段階から介入できる手立てはないかという模索が続いています。
今回取り上げるのは、認知症の治療・予防研究が進むなかで発表された基礎研究の論文です。日本産本わさびに含まれる成分「ヘキサラファン(6-MSITC)」が、アルツハイマー型認知症の原因物質のひとつであるタウタンパク質の異常に対してどのような影響を示したかを、マウスモデルで検証した内容を解説します。
この記事で分かること
- ヘキサラファンがタウの異常なリン酸化を抑えることが細胞・動物実験で確認された
- 抑制の仕組みは従来の抗酸化経路(NRF2)とは別経路で、PP2A(ブレーキ役)を活性化するというもの
- 経口投与で脳に届き、血中バイオマーカーp-tau217の低下や認知・運動機能の改善も報告された
背景:アルツハイマーに関わる2つのタンパク質
アルツハイマー型認知症の発生メカニズムとして広く支持されている考え方に、「アミロイドカスケード仮説」があります。アミロイドカスケード仮説では、脳内で2つのタンパク質──アミロイドβとタウ──が異常をきたし、連鎖的に神経細胞を破壊していくとされています。
注目すべきは、病理変化が症状の出現よりもはるかに早く始まっている点です。アミロイドβの蓄積は発症の約20年前から、タウの異常(神経原線維変化)は約10年前から進行していることが報告されています。つまり、「もの忘れが気になる」と自覚した時点では、脳内の変化はすでに長期間にわたって進んでいるということです34。
では、2つのタンパク質はそれぞれどのように脳を蝕んでいくのでしょうか。
最初に起きるのが、アミロイドβの蓄積です。脳内に「アミロイドβ」という不要なタンパク質が少しずつたまっていきます。健康な脳ではアミロイドβを自然に分解・排出できますが、アルツハイマー型認知症ではアミロイドβの分解・排出処理がうまく働かなくなり、「老人斑」と呼ばれるシミのような塊として蓄積してしまいます。アミロイドβの蓄積だけで広範な神経細胞の障害が起きるわけではありません。問題は、アミロイドβの蓄積がタウの異常を引き起こす引き金になることにあります。
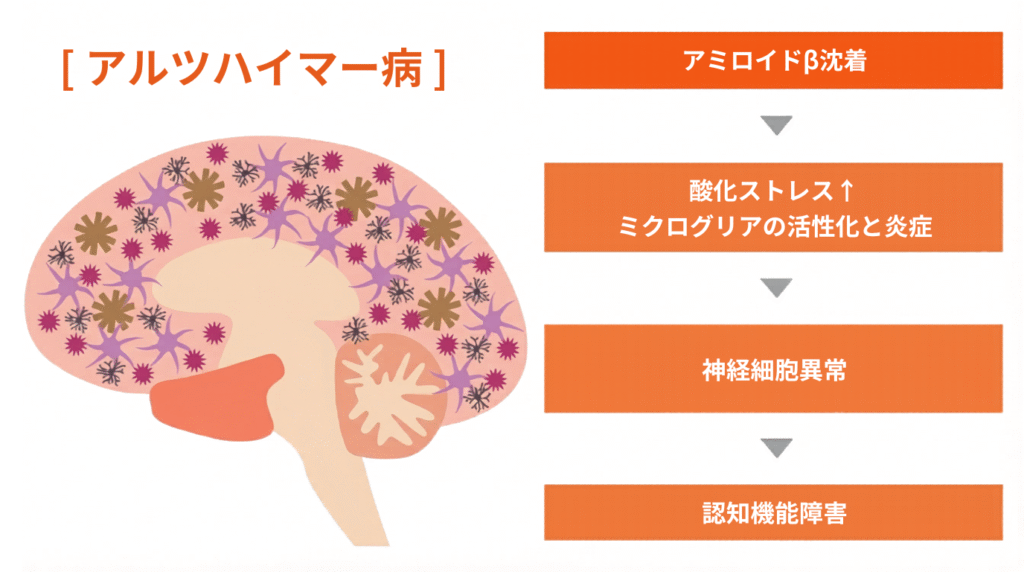
アミロイドβの蓄積によって引き起こされるのが、タウタンパク質の過剰なリン酸化です。タウはもともと神経細胞の骨格(微小管)を安定させる大切なタンパク質です。「リン酸化」という化学的な変化が過剰に起きると、タウは微小管から剥がれ落ちます。剥がれ落ちたタウは「神経原線維変化」という異常な塊を細胞内に形成します。神経原線維変化が起きた神経細胞は機能を失い、やがて死滅します。結果として脳が萎縮し、記憶をつかさどる海馬から順に機能が失われていきます。
タウのリン酸化は「アクセル」と「ブレーキ」で調整されている
タウのリン酸化は、車にたとえると「アクセル」と「ブレーキ」のバランスで制御されています。
- アクセル役(キナーゼ): タウにリン酸基をくっつける酵素(GSK-3β、CDK5など)
- ブレーキ役(ホスファターゼ): タウからリン酸基を外す酵素。中でもPP2Aは、脳内のタウ脱リン酸化の約70%を担う最大のブレーキ役です5。
健康な脳では、アクセルとブレーキがバランスよく働いています。しかし、アルツハイマー型認知症の脳では、ブレーキ役であるPP2Aの働きが低下していることがわかっています。ブレーキが弱くなった結果、タウのリン酸化が止まらなくなってしまうのです。
これまでの治療研究では、「アクセルを弱める」(リン酸化を進める酵素を抑える)アプローチが主流でしたが、十分な成果は得られていません。そこで注目されているのが、「弱くなったブレーキを回復させる」という、新しいアプローチです。

「ブレーキ強化」の鍵を握るヘキサラファン
では、弱くなったPP2Aというブレーキを回復させる物質は存在するのでしょうか。その有力な候補として浮上しているのが、日本産の本わさび(Wasabia japonica)に含まれる天然の辛味成分「ヘキサラファン(6-MSITC)」です。正式には「イソチオシアネート」という種類の化合物に分類されます。
これまでの研究で、ヘキサラファンには以下のような特性が報告されてきました。
- 細胞の防御スイッチ(NRF2経路)を活性化し、体内の抗酸化・抗炎症の力を高める
- 動物実験で神経を保護する作用が確認されている
- 毒性が低く、安全性の面でも注目されている
アルツハイマー型認知症の「アミロイドβの蓄積」に対しては、ヘキサラファンがNRF2経路を通じて一定の効果を示すことが、動物実験で報告されていました 6 7。しかし、もうひとつの原因である「タウタンパク質のリン酸化」に対して、ヘキサラファンが効くかどうかは、これまで調べられたことがありませんでした。今回の論文は、この未検証の領域に踏み込んだ研究です。
研究で分かったこと
1. 細胞実験:ヘキサラファンがタウの異常リン酸化を抑えた
アルツハイマー型認知症モデルマウスの神経細胞を使った実験では、ヘキサラファンを加えることで、病的なタウのリン酸化の指標(AT8、PHF1)が用量に応じて低下することが確認されました。興味深いことに、抗酸化経路(NRF2)を持たない細胞でも、NRF2を持つ細胞と同程度のタウのリン酸化低下が見られました。このことから、ヘキサラファンによるタウのリン酸化の抑制はNRF2とは別の仕組みで起きていると考えられています。
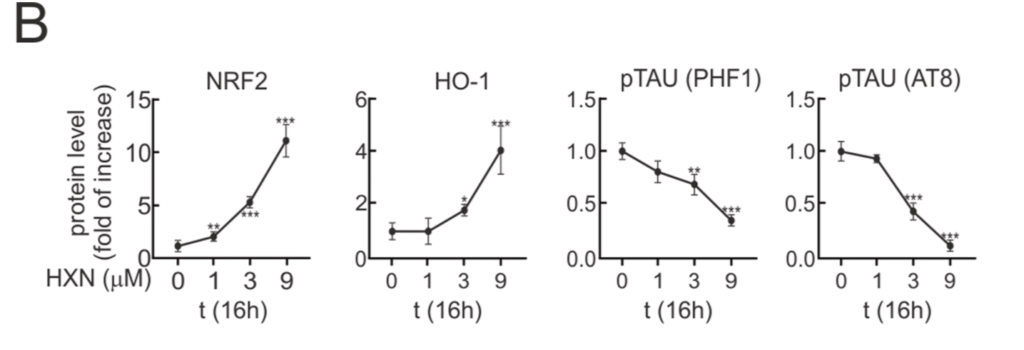
(出典:García-Yagüe AJ et al., Redox Biology 92, 104107 (2026), Fig. 1B より引用)
図の見方:4つのグラフはそれぞれ異なるタンパク質を測定したもの。ヘキサラファン(HXN)投与量の増加に伴い、抗酸化タンパク質(NRF2・HO-1)は上昇し、病的タウのリン酸化の指標(PHF1・AT8)は用量依存的に低下している。
2. 仕組みの解明:「ブレーキ役」PP2Aの活性化
研究チームがさまざまな実験で調べた結果、以下のことが明らかになりました。
- ヘキサラファンの効果は、従来注目されていたGSK-3β(アクセル役)を抑えることでは説明できない 8
- その代わりに、PP2A(ブレーキ役)の活性を高めることでタウの脱リン酸化を促進している
- PP2Aの働きを人工的に止めると、ヘキサラファンの効果も消える
つまり、ヘキサラファンは「アクセルを緩める」のではなく、「ブレーキを強化する」という、これまでとは異なるアプローチでタウの異常を抑えていると考えられます。
3. 脳に届くことを確認
ヘキサラファンをマウスに経口投与したあと、脳内の成分濃度を測定した結果が以下のとおりです。
| 脳の領域 | ピーク濃度 | 到達時間 |
|---|---|---|
| 大脳新皮質 | 約20 ppb | 30分〜1時間 |
| 脳幹 | 12〜15 ppb | 30分〜1時間 |
| 海馬 | 4〜6 ppb | 30分〜1時間 |
経口摂取したヘキサラファンが血液脳関門(脳を守るバリア)を通過して脳内に届くことが確認されました。ヘキサラファンの脳内での滞在時間は約1〜2時間と短いものの、繰り返し摂取することで治療効果が得られる可能性が示されています。
4. 動物実験:脳内と血液中の両方でタウ指標が改善
アルツハイマー型認知症モデルマウスに5週間ヘキサラファンを経口投与した結果、以下のような変化が報告されています。
タウ関連の変化:
- 大脳新皮質・脳幹・海馬のいずれの領域でも、病的タウのリン酸化の指標が低下
- 血液中のp-tau217も統計的に意味のある水準で低下しました。p-tau217はアルツハイマー型認知症の早期診断バイオマーカーとして注目されている指標です9
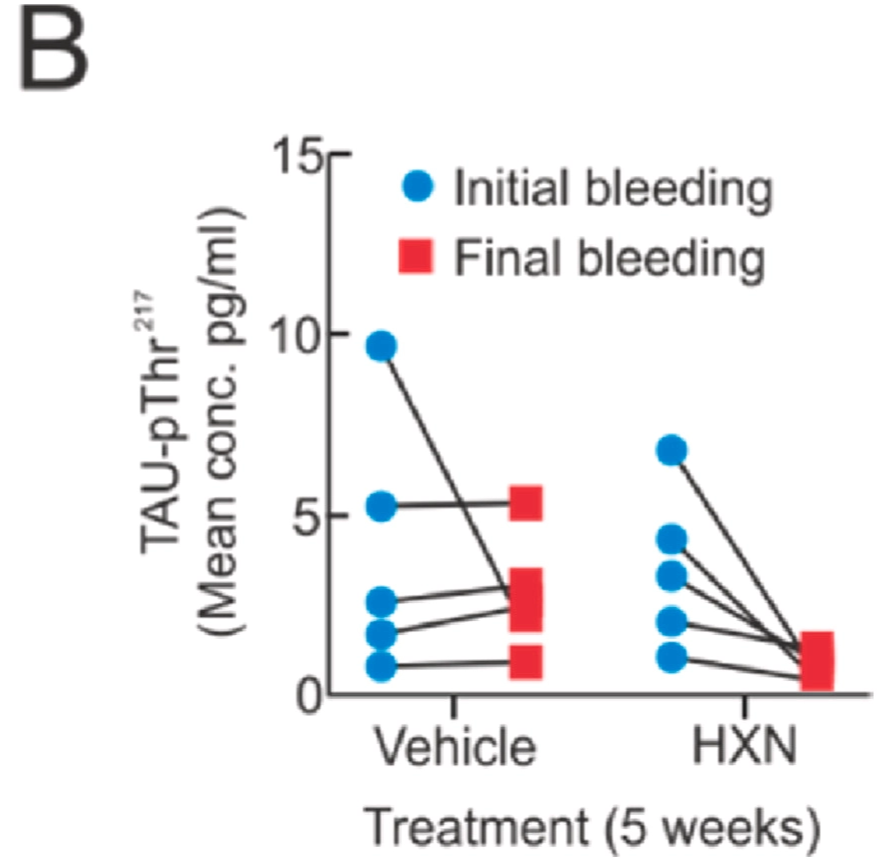
図の見方:縦軸がp-tau217の濃度。各点が1匹のマウスを表し、線で投与前後を結んでいます。ヘキサラファン投与群(6-MSITC)では、投与前に比べて投与後(Treatment)の値が下がっている個体が多いことが見てとれます。
脳の炎症への影響:
- 大脳新皮質と脳幹では、炎症に関わるマーカー(COX2、IL-1β、IL-6など)の低下が確認されました
- 脳の免疫を担うグリア細胞(アストロサイト、ミクログリア)が、炎症に関わる活性化状態から静止状態に戻る傾向も見られました
- 一方、海馬では大脳新皮質ほどの炎症抑制効果は確認されませんでした。海馬へのヘキサラファンの到達量が大脳新皮質の約4分の1と少ないことが、その一因と考えられています
神経細胞の保護とアミロイド病態:
- 神経細胞の健全性を示すカルビンジンD28kの発現が保たれていました
- 大脳新皮質ではアミロイドβプラークの数が約50%減少したという結果も得られています
5. 認知・運動機能への影響
10ヶ月齢のモデルマウスに6週間投与した実験では、以下のような機能面の変化が報告されています。
- 記憶テスト(新しい物体を認識できるか): 識別スコアが2.0〜2.5倍に向上
- トレッドミル試験: 投与3週目から運動パフォーマンスの改善が見られ、5週目まで持続
- シナプス可塑性(海馬の長期増強): 神経細胞どうしの情報伝達効率が回復
ヘキサラファンの2つの作用経路
ここまでの研究結果から、ヘキサラファンには2つの独立した作用経路があると考えられています。
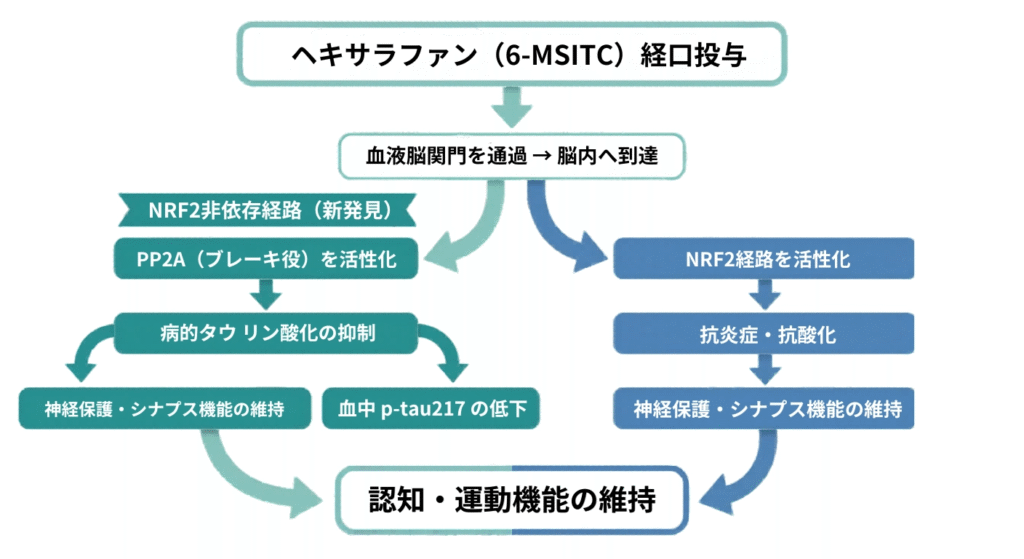
- PP2A経路(NRF2非依存): ブレーキ役の酵素を活性化し、タウの脱リン酸化を促進する
- NRF2経路: 細胞の抗酸化・抗炎症防御を強化する
タウオパチーモデルにおいて、脳内のタウ指標と血液中のp-tau217の両方が低下し、さらに、認知・運動機能の改善まで確認された報告は、本論文が初めてです。
今後の課題
本研究はマウスを用いた基礎研究の段階です。ヒトでの効果を確認するにはさらなる検証が必要です。論文では以下の3点が今後の課題として挙げられています。
- タウの凝集体(固まり)への影響は直接評価されていない
- PP2Aを活性化する分子レベルの仕組みはまだ解明されていない
- 長期的な安全性の評価や、ヒトでの臨床試験への展開が必要
考察:この研究から見えてきたこと
アルツハイマー型認知症の創薬研究では、アミロイドβの除去やタウのリン酸化を進めるキナーゼ(アクセル役)を抑える戦略が主流でした。しかし、臨床試験で十分な成果が得られたケースは限られていました。本研究が提示した、「PP2Aを活性化してブレーキ機能を回復させる」というアプローチは、従来とは異なる方向からの試みで、探索の幅を広げるものと言えます。
また、本研究のデザインの実用性は注目に値します。合成化合物ではなく食品由来の成分を使い、経口投与で脳に届き、効果を血中バイオマーカー(p-tau217)で追跡できました。食品由来成分・経口投与・血中バイオマーカーによる追跡という3条件がそろうと、ヒトでの臨床試験を設計するハードルが大きく下がります。p-tau217は現在、レカネマブなど抗体医薬の治験でも主要評価項目に採用されつつある指標であり、既存の臨床評価基盤にそのまま乗せられる可能性があります。
一方で、冷静に見るべき点もあります。マウスの脳重量はヒトの約0.04%にすぎません。本研究で確認された海馬への到達濃度(4〜6 ppb)がヒトの脳でも再現できるかは未知数です。また、PP2Aは脳以外の臓器でも広く働く酵素であり、全身的な活性化が予期しない影響をもたらすリスクについても検討が必要です。
基礎研究の一報ではありますが、認知症の社会的コストが年間十数兆円規模に達するなかで、研究の選択肢は多いほうがよいのも事実です。従来とは異なる方向からアプローチできる天然成分の候補が見つかったという点で、今後の検証がどのように進むのか、引き続き注目していきたいと思います。
[ 引用・参考文献 ]
本記事の主要論文:
- García-Yagüe AJ et al. “Hexaraphane as a potential therapeutic strategy for tauopathies” Redox Biology 92, 104107 (May 2026) DOI
本文中の引用:
- 厚生労働省「認知症及び軽度認知障害(MCI)の高齢者数と有病率の将来推計」(令和5年度 老人保健事業推進費等補助金、九州大学 二宮利治教授)2024年5月 ↩︎
- Sado M et al. “The estimated cost of dementia in Japan, the most aged society in the world.” PLOS ONE 13(11): e0206508 (2018) ↩︎
- Jack CR Jr. et al. “Hypothetical model of dynamic biomarkers of the Alzheimer’s pathological cascade” Lancet Neurology 9(1): 119-128 (2010) ↩︎
- Bateman RJ et al. “Clinical and Biomarker Changes in Dominantly Inherited Alzheimer’s Disease” New England Journal of Medicine 367: 795-804 (2012) ↩︎
- Qian W et al. “PP2A regulates tau phosphorylation directly and also indirectly via activating GSK-3beta” J Alzheimers Dis 19(4), 1221-1229 (2010) ↩︎
- Morroni F et al. “Protective effects of 6-(Methylsulfinyl)hexyl isothiocyanate on Aβ(1-42)-Induced cognitive deficit, oxidative stress, inflammation, and apoptosis in mice” Int J Mol Sci 19(7) (2018) ↩︎
- Uruno A et al. “Nrf2 suppresses oxidative stress and inflammation in App Knock-In Alzheimer’s Disease model mice” Mol Cell Biol 40(6) (2020) ↩︎
- García-Yagüe AJ et al. “Dual targeting of Keap1 and Gsk-3 by hexaraphane in the regulation of transcription factor Nrf2” Free Radic Biol Med 239, 579-593 (2025) ↩︎
- 本論文 Discussion 内引用 ↩︎